DIABETES MODY: REPORTE DE
4 CASOS
JavieR ChiaRpenello*1-2, M. ailén vidal3, ana lauRa Baella1, Julia Bonino3, MaRía viCtoRia pent MaRia3, viRginia seRMasi3, MaRía de las nieves lauRenti3, Castagnani, v.1
1) Servicio
de Endocrinología del Hospital Centenario de Rosario.
2) Centro
de Endocrinología de Rosario.
3) Concurrente
del Servicio de Endocrinología de Rosario.
Recibido:
20-8-2019
Aprobado para su publicación: 11-3-2020
Resumen
Con el término diabetes
MODY (Maturity Onset Diabetes of the Young) se
denomina a un grupo heterogeneo de enfermedades monogénicas, que presentan en común una disfunción de las células
b. Se conocen en la actualidad más
de 800 mutaciones relacionadas a este
tipo de diabetes. La más común
es la diabetes MODY 2 debida a una
mutación dentro del
gen de la glucoquinasa. Su prevalencia se estima entre
el 2-5% de los tipos
de diabetes no insulinorequirientes. El presente trabajo
describe cuatro mutaciones de diabetes MODY (tres tipo 2 y una tipo 3)
diagnosticadas en el Servicio de Endocrinología Infantil
del Hospital Centenario de la ciudad
de Rosario, Santa
Fe. Argentina.
Palabras claves: MODY, gen glucoquinasa, diabetes, HNF1A, mutación.
DIABETES MODY: REPORT OF FOUR CASES
Abstract
With the term diabetes MODY (Maturity Onset Diabetes of the Young) is called a heterogeneous group of monogenic diseases, which present in common a dysfunction of b cells. There are currently
more than 800 mutations related
to this type of diabetes. The most common
is MODY 2 diabetes due to a mutation within
the glucokinase gene. Its prevalence
is estimated between
2-5% of non-insulin-dependent diabetes types. The present
work describes four MODY diabetes mutations (three type 2 and one type 3) diagnosed in the Child
Endocrinology Service of the Centenario Hospital of the city of Rosario, Santa Fe, Argentina.
Key words:
* Correo electrónico: jchiarpenello@hotmail.com
Introducción
La diabetes MODY (Maturity Onset Diabetes of the Young) es un
grupo genéticamente y clínicamente heterogéneo
de enfermedades monogénicas, de herencia autosómica dominante, que se
caracterizan por la disfunción
de las células b.1,2 La hiperglucemia suele
aparecer antes de los 25 años y se asocia
con defectos primarios en la
secreción de insulina.
En general
en estos tipos de diabetes
los pacientes no son obesos
(lo que nos ayuda a diferenciarlos clínicamente de la diabetes mellitus
tipo 2), al igual que no
suelen tener complicaciones
vasculares y no requieren tratamiento medicamentoso.3-5
Aunque se desconoce
la prevalencia exacta de MODY, se estima que estas variantes son responsables
del 2 al 5% de todos los casos
de diabetes no insulinorequiriente. Hay más de 800 mutaciones
conocidas asociadas con MODY y otras nuevas
se están descubriendo.3 La mayoría de los casos
se deben a mutaciones
heterocigotas en 6 genes 6,7 (ver cuadro
N°1).
Cuadro N°1:
Subtipos de diabetes MODY.
A continuación se exponen los casos de cuatro pacientes
en los cuales se les realizó el diagnóstico (mediante el estudio genético) de MODY 2 en 3 de ellos
(2 de ellas son hermanas) y de MODY
3 en el restante.

Para el estudio genético
se realizó una extracción
de ADN a partir de muestra obtenida
y se amplificó mediante PCR de la región flanqueante a la mutación. Luego se preparó
las reacciones de secuenciación de ADN
y electroforesis capilar
y se analizó de manera
bioinformática las secuencias obtenidas por comparación con las secuencias de referencia.
Casos clínicos
Paciente 1:
Paciente de 5 años y 4 meses
derivada al consulto- rio de Endocrinología Pediátrica por registros de hiperglucemia de ayuno en laboratorio de rutina.
Antecedentes personales: recién nacida a término (RNT), peso al nacer (PN): 3.150 grs., comunicación interauricular.
Antecedentes familiares: tío paterno con diabetes en tratamiento
con hipoglucemiantes orales. Se desconocen antecedentes patológicos de padres y hermanos.
Examen físico: Peso (P): 23,600
kg. (Percentil (P) 90-97, gráficos
de Lejarraga y Orfla),8 Talla (T): 117,5 cm. (P 90-97) e índice masa corporal (IMC):
17,09 (DS +1). No presenta
acantosis nigricans, y el resto del
examen general sin hallazgos patológicos.
El laboratorio al diagnóstico se observan en el cuadro N° 2.
Se indica plan
alimentario para diabetes y auto- monitoreo glicémico, cuyos
valores en promedio
son: en ayunas 110-136
mg/dl, pre-almuerzo 116-150
mg/dl y pre-cena
120-150 mg/dl.
Ante la ausencia de síntomas
de descompensación diabética y por presentar hiperglicemias leves y persistentes se sospecha diagnostico de
diabetes MODY por lo
que se solicita estudio molecular del gen de glucoquinasa (GCK) (ver cuadro N°2). Corresponde a una nueva mutación no descripta al momento en la literatura.
Se solicita estudio
genético y laboratorio a los familiares de primer grado.
Encontrándose la misma
mutación del gen de la glucoquinasa en el padre. La madre y
el hermano (que comparten ambos
padres) no presen- tan dicha mutación.
Paciente 2:
Niña de 9 años
y 7 meses. P: 33,2
kg. (P 50-75) T:
142,4 cm. (P
90-97). IMC: 16,37 (DS 0).
Antecedentes personales: RNT, PN 2.700 grs. Hiperbilirrubinemia neonatal transitoria, necesitando ingreso
a sala de neonatología durante
los primeros 4 días de vida.
Antecedentes familiares: Padre de 38 años de edad, con
diagnóstico de diabetes mellitus en su adolescencia, refiere nunca
haber requerido tratamiento medicamentoso así como tampoco internaciones por descompensaciones de la diabetes. Tía paterna
de 19 años de edad, diabética tipo 1, quien presenta anticuerpos anti-GAD positivos,
en tratamiento con insulina.
El laboratorio al diagnóstico se observan en el cuadro N° 2.
Paciente 3:
Esta paciente es hermana de la paciente 2.
Niña de 7 años
y 10 meses. P: 20 kg. (P 10). Talla:
118 cm. (P 10-25).
IMC: 16,36 (DS 0 y +1).
Antecedentes personales: RNT. PN: 3.050 grs. Actualmente con diagnóstico de asma intermitente y síndrome anémico.
Antecedentes familiares: ver
paciente 2.
Ambas hermanas presentaban registros de hiperglucemias
leves/moderadas como hallazgos de laboratorio
en los últimos 6 meses.
Ninguna de las dos hermanas
presentaron síntomas o signos
de descompensación diabética. Se les solicita a ambas
estudio genético para MODY. Ambas
presentaron una mutación no descripta
en la literatura al momento de su publicación1 (ver cuadro n°2).
El laboratorio al diagnóstico se observan en el cuadro N° 2.
Para más información de la paciente 2 y 3 (hermanas)
sugerimos consultar su publicación anterior.1
Paciente 4:
Consulta por hiperglucemias al Servicio de Endocrinología
derivado por su médico de cabecera con 11 años y 9 meses de edad.
Antecedentes personales: recién nacido de pretérmino
(edad gestacional: 36 semanas) PN: 3.270 grs., con diagnóstico neonatal de reflujo
gastroesofágico.
Antecedentes familiares: padre con diagnóstico de diabetes mellitus.
A los 11 años por un cuadro gastrointestinal presentó glucemias en ayunas con valores
entre 98 a 130 mg/dl por
automonitoreo glucémico; niega polidipsia, poliuria y pérdida de peso.
En la consulta: P: 35,8 kg. (P 25-50),
T: 143 cm. (P 25-50), IMC: 17,5 (DS 0). Se indica plan alimentario para
diabetes, automonitoreos glucémicas.
Además, se solicita
laboratorio (ver cuadro n°2). De acuerdo a los
resultados de los mismos
y ante la sospecha
diagnóstica se decide
realizar estudio
genético para MODY 2 y 3.
Al paciente
se le diagnostica diabetes MODY 3 con una mutación
no descripta al momento
de esta publicación.
También se les solicitan laboratorios y estudio
genético a padres y hermanos para búsqueda
de la mutación. Madre y hermanos negativos para la mutación. El padre se niega a realizar dicho estudio.
Para otros
detalles de laboratorio y estudio genético ver cuadro n° 2.
Discusión
En esta
publicación describimos 4 casos de variantes MODY, de los
cuales 3 de ellos son
MODY 2 y uno de ellos MODY 3, todas diagnosticadas a través del estudio genético correspondiente.
La diabetes
MODY es una forma de presentación de diabetes que en los últimos años ha aumento
su incidencia. Se han hallado diferentes mutaciones que dan origen a distintos subtipos
de MODY; de ellas las mutaciones del gen glucoquinasa (MODY 2) es considerada
la más prevalente.9,10
Se estima
que las mutaciones de este gen están presentes en aproximadamente 1 de cada
1.000 personas, pero la mayoría lo desconoce;11 al igual
que en el 1-2% de las
diabetes gestacionales.
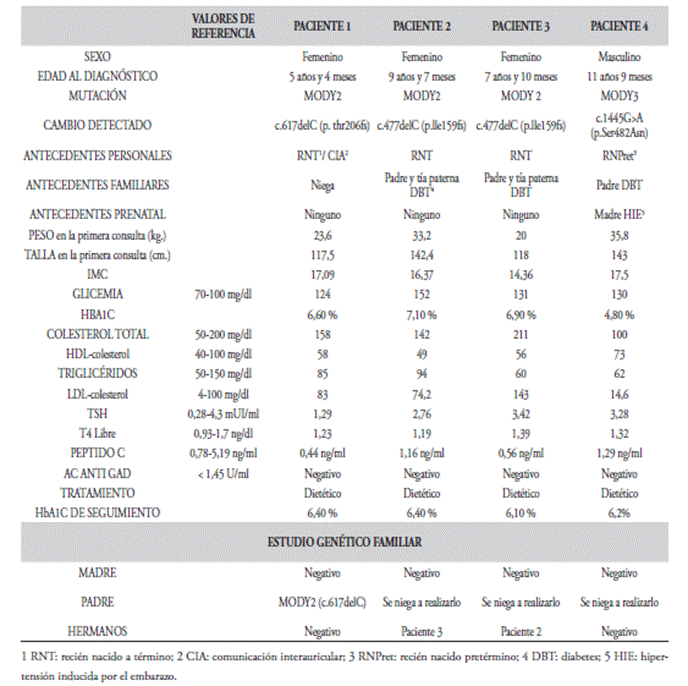
Cuadro N° 2: características clínicas,
de laboratorio y estudio molecular
para diabetes MODY de los cuatro pacientes
descriptos.
El modo
de presentación es a través
de hiperglicemias leves a moderadas
que determinan una hemoglobina glicosilada A1c generalmente menor
a 7,5%. Estos pacientes no son obesos,
requieren en general
sólo trata- miento dietético y actividad física
para mantener niveles
de glucosa adecuados (si bien en algunos casos
pueden requerir tratamiento medicamentoso para lograr un adecuado control glucémico) y tienen
una historia fa- miliar de diabetes, como podemos correlacionar con otras publicaciones al respecto.3 Asimismo, es de des-
tacar que estos pacientes suelen tener un perfil lipídico que contribuye a la baja
frecuencia de complicaciones cardiovasculares.
Los pacientes que
tienen hecho un diagnóstico de diabetes MODY 2 (por mutación del gen de la glucoquinasa) presentan igualmente riesgo de desarrollar diabetes mellitus tipo 1 o 2 como el resto
de la población. Se debe
considerar la aparición concomitante de alguno
de estos dos últimos tipos
de diabetes en aquellos en los que encontramos la hemoglobina
glicosilada A1c mayor a 7,6% (límites de confianza del 95% en la diabetes MODY-mutación de la glucoquinasa) en reiteradas oportunidades.13
En relación
a los pacientes con este tipo de diabetes (que
describimos en el presente trabajo) algunos trabajos no recomiendan realizar
el fondo de ojos en forma rutinaria (si bien esto se encuentra en discusión), y solo indicar su realización en los casos que se acompañe de diabetes mellitus tipo 1 o 2 concomitante.11
Bibliografía
1.
Chiarpenello
J, Fernández, Riccobene y col. Diabetes Mody
2: reporte de dos casos con nueva mutación en el gen de glucoquinasa. Rev Med Rosario
81: 123-126, 2015.
2.
Velho
G, Frogulel P. Genetic,
metabolic and clinical characteristic of maturity onset
diabetes of a young. Eur J Endocrinol 138:233-239. 1998.
3.
Hattersley A, Bruining J, Shield J y col. ISPAD Clinical
Practice Consensus Guidelines
2006-2007 the diagnosis and management of monogenic diabetes in children
Pediatric diabetes, 7:352-360,2006.
4.
Velho G, Blanche
H, Vaxillaire M y col. Identification of 14
new glucokinase mutations and description of the clinical profile of
42 MODY-2 families, Diabetologia
40:217- 224,1997.
5.
Lopez A, Foscalidi S, Krochik G y col. Glucokinase Gene Mutation Screening in Argentinean Clinically Characterized MODY Patients. Exp Clin Endocrinol Diabetes
117:391- 394, 2009.
6.
Nyunt O, Wu JY, McGown IN,
Harris M y col. Investigating maturity onset
diabetes of the young. Clin Biochem
Rev 30:67-74, 2009.
7.
Williams.
Tratado de endocrinología; 13.a Edición. Elsevier, 2017.
8.
Wędrychowicz A, Tobór E, Wilk M y col. Phenotype Heterogeneity in Glucokinase–Maturity-Onset Diabetes of the Young (GCK-MODY) Patients. Clin Res Pediatr Endocrinol 9:246-252, 2017.
9.
Gomez AE. MODY diabetes: adult-onset type diabetes
in the Young.
Medware, 10(02): e4415,
2010.
10.
Lejarraga H, Orfla G. Estándares de peso y estatura para niñas y niños
argentinos desde el nacimiento hasta la madurez. Arch.
Argent. Pediatr.
85: 209-22, 1987.
11.
Chakera AJ, Steele AM,
Gloyn,Maggie AL y col. Recognition and Management of Individuals With Hyperglycemia
Because of a Heterozygous Glucokinase Mutation. Diabetes
Care; 38:1383–1392, 2015.
12.
Chakera AJ, Spyer G, Vincent N y
col. The 0.1% of the population with glucokinase monogenic diabetes can be recognized by clinical
characteristics in pregnancy: the
Atlantic Diabetes in Pregnancy cohort. Diabetes Care 37:1230-1236, 2014.
13.
Steele AM, Wensley
KJ, Ellard S y col. Use of HbA1c in the
identification of patients
with hyperglycaemia caused
by a glucokinase mutation: observational case control studies. PLoS
ONE;8:e65326. 2013.
Conclusión
Se debe sospechar
DBT MODY en todo niño o adolescente que ha sido diagnosticado como diabético tipo 1,
pero que se presenta con autoinmunidad negativa y persistencia de niveles adecuados de péptido C a
3-5 años del diagnóstico; y en aquellos
pacientes con diagnóstico de diabetes
mellitus tipo 2 que no presentan características de
insulinoresistencia.
![]()

